Kuiv element on lihtsaim elektrienergiaallika vorm. Mitu rakku ühendatud rakku moodustab koos patarei. The pliihape või nikkel-kaadmium aku on kuiva elemendi täiustatud versioon. Selle elemendi leiutas esmakordselt prantsuse insener Georges Leclanche aastal 1866. Tema leiutis nimetati tema nime järgi kui Leclanche patarei. Kuid tol ajal oli see väga raske ja seda sai kergesti murda. Kuivelemendil on sama põhimõte ja see on Leclanche aku täiustatud versioon ning seda saab kasutada erineva pinge ja suurusega. Tsink-süsinikelemendi kaubandusliku vormi, mis on Leclanche patarei modifitseeritud vorm, leiutas 1881. aastal Carl Gassner Mainzist. Seda toodetakse suurtes kogustes ja kasutatakse paljudes rakendustes nagu mänguasjad, raadiod, kalkulaatorid jne.
Mis on kuiv rakk?
Kuiv element on seade, mis toodab elektrit keemiliste reaktsioonide põhjal. Kui elemendi kaks elektroodi on suletud tee kaudu ühendatud, sunnib rakk elektrone ühest otsast teise voolama. Elektronide voog põhjustab voolu suletud ahelas.

Kuivrakukihid
Keemiliste reaktsioonide abil voolavad elektronid ühest otsast teise. Kui kaks või enam õige polaarsusega ühendatud rakku voolab suure potentsiaali tõttu rohkem elektrone. Seda kombinatsiooni nimetatakse akuks. Minimaalsest 1,5 V kuni 100 V pingest alates saab patarei kasutada pingepiirkonna saamiseks. Isegi aku väljund-alalisvoolu pinget saab reguleerida erinevatele tasemetele, kasutades näiteks elektrilisi muundureid hakkija vooluringid.
Lahtri struktuur
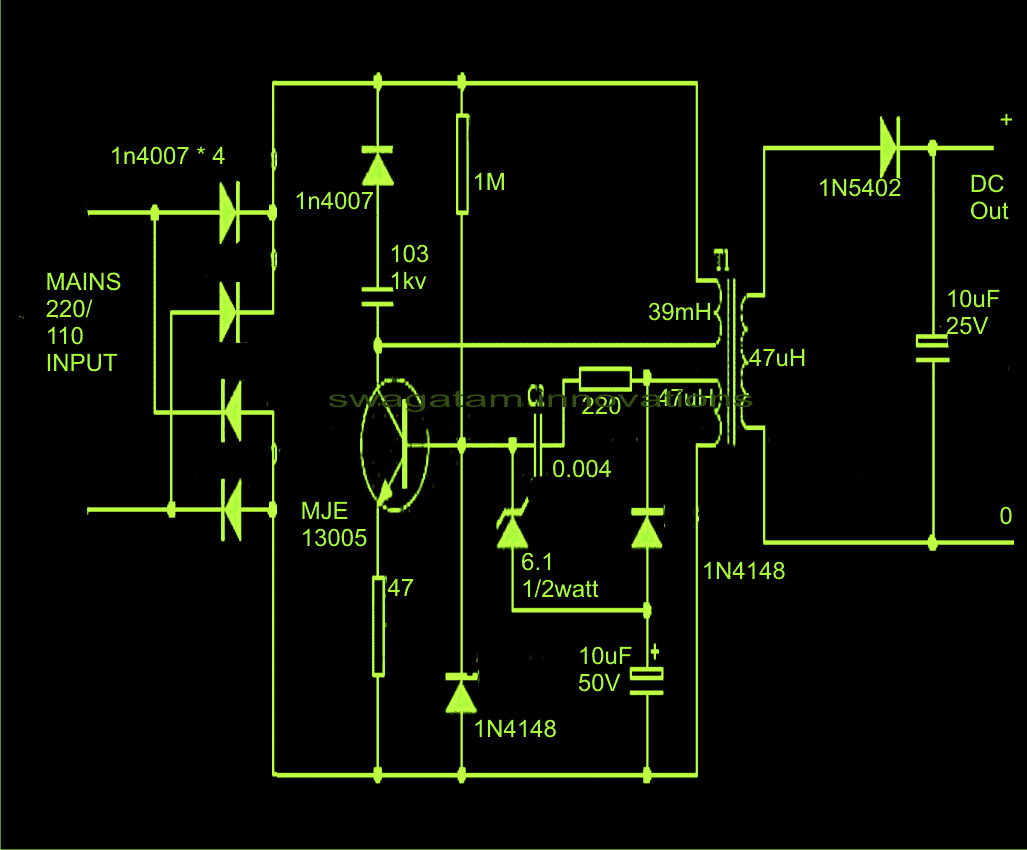
Tsingi-süsiniku kuiva elemendi struktuur on näidatud joonisel. See koosneb anoodklemmist tsinkina või üldiselt grafiitvardana. Süsinik moodustab katoodi klemmi. Võib täheldada, et kuiva elemendi vanemates versioonides kasutati katoodina tsinki ja anooditerminalina grafiiti. Elementide valik põhineb põhimõtteliselt elementide välimise orbiidi keemilisel konfiguratsioonil.

Kuiva raku struktuur
Kui sellel on välisel orbiidil rohkem arvulektrone, võib see toimida doonorina ja moodustab seega katoodi. Samamoodi, kui äärmisel orbiidil on vähem elektrone, suudab see anoodi hõlpsasti aktsepteerida ja moodustada. Nende vahele pandud elektrolüüt toimib keemiliste reaktsioonide katalüsaatorina. Üldiselt kasutame elektrolüüdina ammooniumkloriidi želeed. Näidatud joonisel on kasutatud elektrolüüt tsingi ja kloriidi segu. Naatriumkloriidi kasutatakse ka elektrolüüdina. Anoodvarda ümber on ümbritsetud mangaandioksiidi ja süsiniku segu.
Kogu konfiguratsioon asetatakse metalltorusse. Tarretise kuivamist takistatakse raku ülaosas oleva pigi abil. Altpoolt asetatakse süsinikseib. Selle seibi eesmärk on vältida tsingianoodvarda kokkupuudet anumaga.
Seda nimetatakse ka vahetükiks, nagu skeemil näidatud. Tsingipurki ümbritseb isolatsiooni eesmärgil ka paberist isolatsioon. Suurte patareide jaoks kasutatakse ka muid isoleermaterjale, näiteks vilgukivi jne. Elli positiivne klemm moodustub ülaosas. Raku negatiivne terminal moodustub aluses.
Kuiva raku töötamine
Kuiv rakk töötab põhimõtteliselt keemiliste reaktsioonide kallal. Elektrolüüdi ja elektroodide vahel toimuvate reaktsioonide tõttu voolavad elektronid ühest elektroodist teise. Sellised ained nagu happed lahustuvad vees, moodustades ioniseeritud osakesi. Ioniseeritud osake on kahte tüüpi. Positiivseid ioone nimetatakse katioonideks ja negatiivseid ioonideks. Vees lahustunud happeid nimetatakse elektrolüütideks.
Ülalmainitud diagrammil moodustab elektrolüüdina tsinkkloriid. Samamoodi moodustub ammooniumkloriidi želee ka elektrolüüdina. Elektrolüütidesse sukeldatud metallvardad moodustavad elektroodid. Metallvardade keemiliste omaduste põhjal on meil anoodina positiivne elektrood ja katoodina negatiivne elektrood.
Elektroodid meelitavad vastupidiselt laetud ioone oma küljele. Näiteks meelitab katood anioone ja anood katioone. Selles protsessis voolavad elektronid ühest suunast teise, seega saame laengute voo. Seda nimetatakse praegune .
Keemilised reaktsioonid
Rakus toimuvad reaktsioonid on toodud allpool. Esiteks on oksüdatsioonireaktsioon.

Selles osas oksüdeeritakse tsinkkatood positiivselt laetud tsingiioonideks, vabastades kaks iooni. Neid elektrone kogub anood. Siis tuleb redutseerimisreaktsioon.

Reduktsioonireaktsioon anoodil on näidatud eespool. See reaktsioon tekitab elektrivoolu. See vabastab oksiidioone koos magneesiumoksiidiga. See reaktsioon tekib siis, kui magneesium on ühendatud elektrolüüdiga.


Kaks ülejäänud reaktsiooni kujutavad happe-aluse reaktsiooni ja sadestumisreaktsiooni, mis toimub kuivas rakus. Happe-aluse reaktsioonis kombineeritakse NH koos OH-ga, et saada NH3 koos veega. Tulemused on NH3 ja vesialus.
Erinevus kuiva ja märja raku vahel
Peamine erinevus kuiva ja märja elemendi vahel on elektrolüüdi vorm. Nagu eelnevalt mainitud, on kuivas kambris elektrolüüt nagu ammooniumkloriid oma olemuselt kuiv. Sellised kuivad elemendid on levinumad ja neid kasutatakse mänguasjades, raadioseadmetes jne. Kuid märjas elemendis on elektrolüüt vedelas olekus.
Kasutatakse vedelaid elektrolüüte, näiteks väävelhapet, mis on ohtlik söövitav vedelik. Selliste vedelike olemuse tõttu on märg rakk oma olemuselt plahvatusohtlikum ja sellega tuleb ettevaatlikult ümber käia. Selliste märgade rakkude parim eelis on see, et neid saab hõlpsasti laadida ja kasutada mitmel otstarbel. Sellised patareid leiavad tavalist kasutamist lennunduses, kommunaalteenustes, energiasalvestuses ja mobiiltelefonide tornides.
Kuiva raku funktsioonid
Kuiva elemendi funktsioon põhineb elektroodi ja elektrolüütide vahelistel keemilistel reaktsioonidel. Kui elektroodid asetatakse elektrolüütidesse, meelitab see vastakuti laetud ioone enda poole. See põhjustab laengute voogu ja seega tekib vool.
Eelised
The kuiva elemendi eelised sisaldama järgmist.
- Kuival rakul on mitmeid eeliseid, näiteks
- Selle suurus on väike.
- See võib olla erinevates pingetasemetes.
- See on käepärane ja sellel on arvukalt rakendusi.
- See on ainus alalisvoolu pingeallikas.
- Seda saab kasutada koos elektrooniliste vooluahelatega väljundpinge reguleerimiseks
- See on laetav.
Puudused
The kuiva kambri puudused sisaldama järgmist.
- Seda tuleb käsitleda ettevaatlikult
- See on plahvatusohtlik
- Suured reitinguga patareid on väga rasked
Rakendused
The kuiva kambri rakendused sisaldama järgmist.
- Mänguasjad
- Lennundus
- Mobiiltelefonid
- Raadio
- Kalkulaator
- Kellad
- Kuuldeaparaadid
Seetõttu oleme näinud süsteemi toimimist, klassifitseerimist ja rakendusi kuivad rakud . Üks huvitav punkt, mida tuleb märkida, on see, et aku töötab ainult siis, kui elektroodid on omavahel füüsiliselt kontaktis. Kahe elektroodi vahel peab olema juhtiv keskkond. Küsimus on selles, kas vett saab kasutada juhtiva keskkonnana kuiva elemendi elektroodide vahel? Mis juhtub sel juhul, kui see rakk kastetakse vette?